Règle de Barton
Page 1 sur 1
 Règle de Barton
Règle de Barton
savannah AUGUSTE
10:47 (il y a 19 minutes)
À moi
Bonjour Monsieur,
J'ai une question par rapport à la règle de Barton :
Souvent, on a le choix entre plusieurs substituants pouvant être décrits comme encombrants et déterminer lequel est LE plus encombrant ( histoire de savoir qui mettre en position équatoriale ) ne me paraît pas toujours évident. Auriez-vous des critères à prendre en compte en priorité ou des astuces pour écarter tout doute dans ces situations ?
Merci et bonne journée,
AUGUSTE Savannah
 Re: Règle de Barton
Re: Règle de Barton
Bonjour Savannah,
Il faut revenir à la source de cette règle qui, je le rappelle, indique que la conformation chaise la plus stable est celle qui minimise le nombre de substituants du cycle cyclohexanique en position axiale.
Les deux origines de la destabilisation d'une conformation avec un substituant en position axiale sont les suivantes :
1/ interaction 1,3-diaxiale avec intervention d'une gêne stérique entre substituants axiaux du même côté du plan moyen du cycle (notamment si deux substituants volumineux coexistent) :

2/ Interaction gauches avec le squelette du cycle :
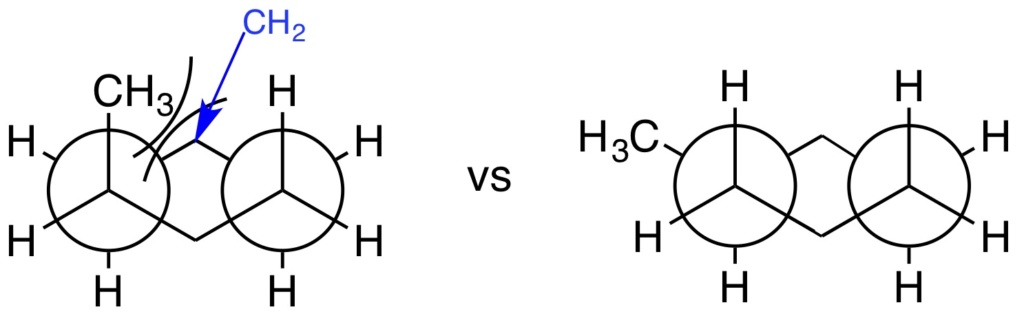
Dans les deux cas, plus le substituant est "volumineux", plus la destabilisation due à ces interactions est grande.
On dispose en réalité, pour les cyclohexanes monosubstitués, de tables qui précisent l'énergie de destabilisation selon le substituant, qui s'appelle "énergie d'Eliel". Cela donne une réponse claire à ta question (source : March Organic Chemistry) :
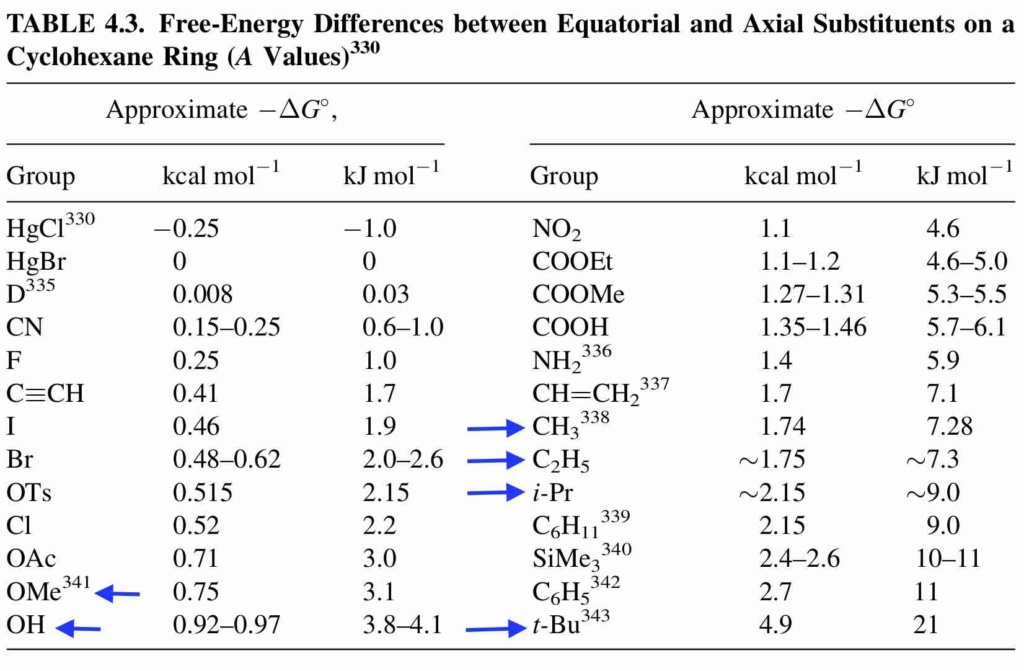
Par exemple, on voit qu'entre Me, Et et iPr, peu de différence, mais par contre tBu : très volumineux.
Plus surprenant : Me plus volumineux que OMe (le groupement CH3 est loin des autres substituants du cycle car non branché directement dessus).
C6H5 = Ph : pas tellement plus volumineux que Me, car il est plan.
Voila les tendances !
Bonne journée,
AM
Il faut revenir à la source de cette règle qui, je le rappelle, indique que la conformation chaise la plus stable est celle qui minimise le nombre de substituants du cycle cyclohexanique en position axiale.
Les deux origines de la destabilisation d'une conformation avec un substituant en position axiale sont les suivantes :
1/ interaction 1,3-diaxiale avec intervention d'une gêne stérique entre substituants axiaux du même côté du plan moyen du cycle (notamment si deux substituants volumineux coexistent) :

2/ Interaction gauches avec le squelette du cycle :

Dans les deux cas, plus le substituant est "volumineux", plus la destabilisation due à ces interactions est grande.
On dispose en réalité, pour les cyclohexanes monosubstitués, de tables qui précisent l'énergie de destabilisation selon le substituant, qui s'appelle "énergie d'Eliel". Cela donne une réponse claire à ta question (source : March Organic Chemistry) :

Par exemple, on voit qu'entre Me, Et et iPr, peu de différence, mais par contre tBu : très volumineux.
Plus surprenant : Me plus volumineux que OMe (le groupement CH3 est loin des autres substituants du cycle car non branché directement dessus).
C6H5 = Ph : pas tellement plus volumineux que Me, car il est plan.
Voila les tendances !
Bonne journée,
AM
Page 1 sur 1
Permission de ce forum:
Vous ne pouvez pas répondre aux sujets dans ce forum|
|
|
